Blog de Notícias
A causa dessas doenças musculares pode variar de uma interrupção da inervação e destruição dos segmentos das fibras musculares, a alterações nas funções de enzimas ou proteínas dentro das fibras, o que caracteriza doenças musculares de ordem estrutural.
O diagnóstico de doenças musculares é considerado difícil, mas o exame clínico cuidadoso dos pacientes e o desenvolvimento de técnicas laboratoriais avançadas, trouxe maior precisão e agilidade a estes diagnósticos.
A Biopsia Muscular pode confirmar de forma objetiva a presença de denervação, inflamação ou até mesmo toxicidade medicamentosa. Este procedimento também possibilita identificar a presença de estruturas anormais e/ou anormalidades em expressões proteicas que, quando correlacionados com informações clínicas adequadas, pode auxiliar na identificação das causas.
Para conseguir uma boa conduta e tratamento adequado da doença muscular, é essencial que haja uma estreita colaboração entre o neurologista ou reumatologista, o neuropatologista e o geneticista. Uma compreensão geral das diferentes disciplinas envolvidas nessa avaliação é essencial e uma comunicação eficaz entre os profissionais envolvidos é de grande importância para uma conduta efetiva.
Referência:
GOEBEL, H.H. SEWRY, C.A. WELLER, R.O. Muscle Disease: Pathology and Genetics. Second Edition. Basil: ISN Neuropath Press, 2013.
Os Tumores Metastáticos do Sistema Nervoso Central [SNC] são tumores que se originam fora do SNC e dispersam-se predominantemente pela via hematogênica para o SNC. Menos frequentemente também podem invadir SNC a partir da infiltração de estruturas anatômicas adjacentes.
A incidência de metástases de tumores para o SNC é provavelmente subestimada, mas vem aumentando significativamente na última década. Este aumento se deve ao avanço das tecnologias diagnósticas, que permitem maior precisão diagnóstica aos casos reportados.
A fonte mais frequente de metástases cerebrais em adultos é o câncer de pulmão, seguido por câncer de mama, melanoma, carcinoma de células renais e câncer colorretal. Próstata, mama e pulmão são os tipos de câncer mais comuns que geram metástases para a coluna. Em crianças as fontes mais comuns de metástases para o SNC são leucemias e linfomas.
Os sintomas neurológicos de metástases intracranianas são geralmente o aumento da pressão intracraniana ou um efeito local do tumor no tecido encefálico adjacente. Os sintomas podem progredir gradualmente e incluir dor de cabeça, paresia (perda de força), ataxia (incoordenação), alterações visuais, náuseas e distúrbios sensoriais.
Os principais fatores prognósticos estabelecidos para metástases cerebrais são a idade do paciente, número de metástases cerebrais, status da doença primária, tipo de tumor e suas características moleculares. Em estudos recentes, a sobrevida de pacientes com metástases do SNC pode ser atribuída à melhoria de tratamentos focais e sistêmicos em combinação com diagnósticos precoces e objetivos.
FONTE: LOUIS, D. et al. WHO Classification of Tumours of the central Nervous System. 4th Ed. IARC: Lyon, 2016.
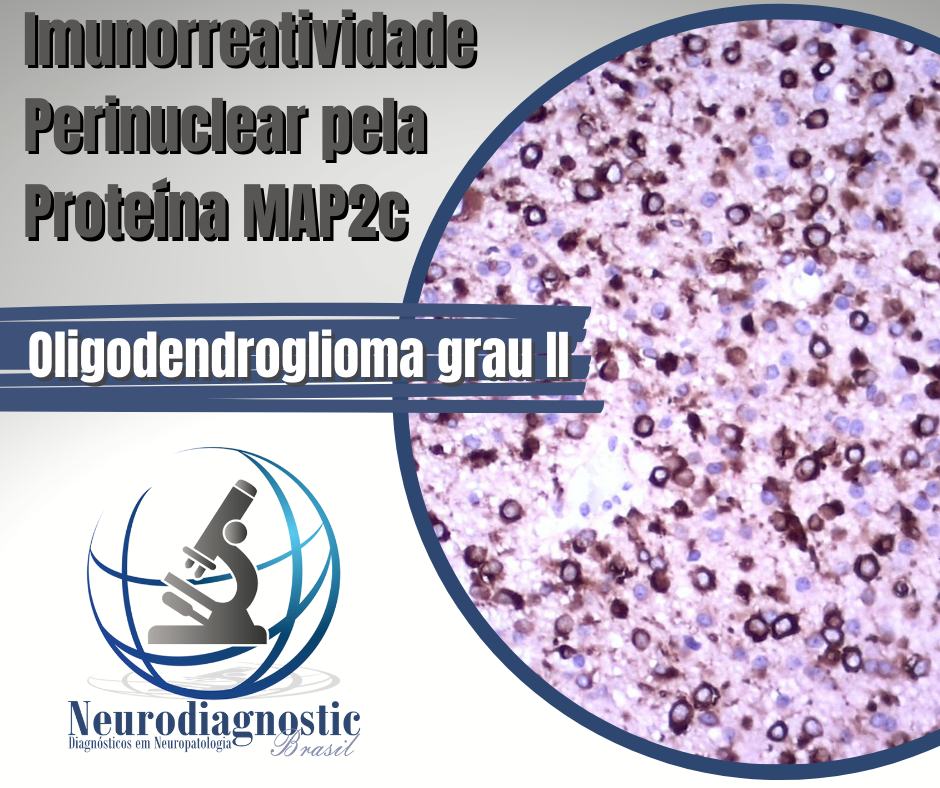
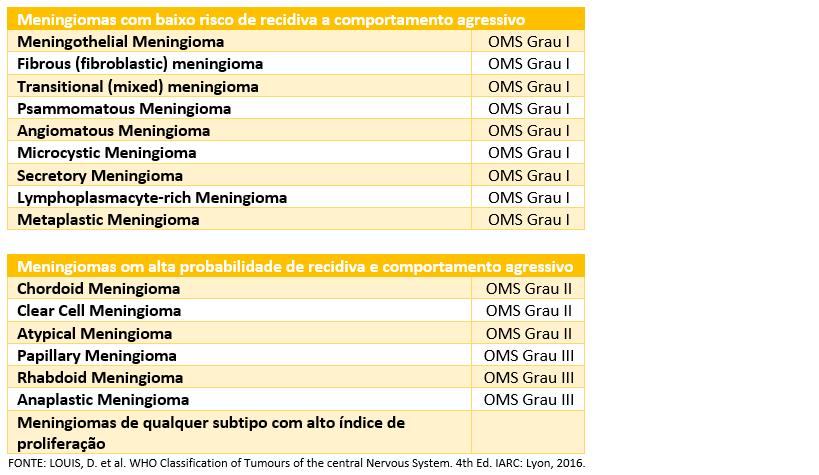
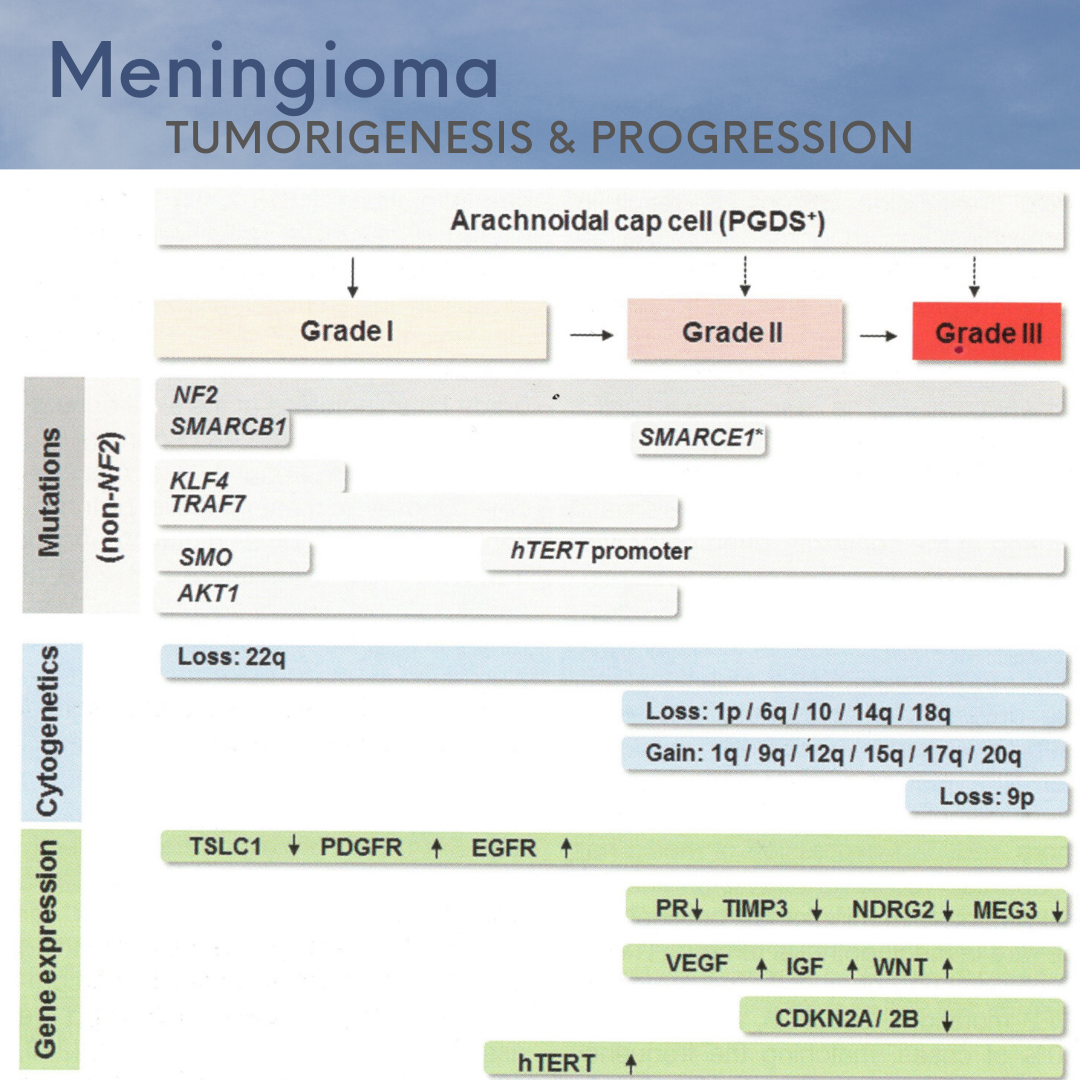
É um grupo de neoplasias que, em sua maioria, são benignas e de baixo crescimento. Alguns poucos subtipos podem possuir combinações de parâmetros morfológicos que estão associados com desfechos clínicos menos favoráveis. Estes subtipos podem corresponder histologicamente aos graus II e III.
A média de idade de pacientes com meningioma é de 65 anos e o risco de possuir tal lesão aumenta com a idade. Os sintomas mais comuns ocorrem devido à compressão de estruturas adjacentes, com déficits específicos que dependem da localização do tumor. Dores de cabeça e crises epiléticas são comuns (mas não específicas).
Estudos mostram que cerca de 20% dos meningiomas recidivam em 20 anos. Os principais fatores de recidiva são a extensão da ressecção, que pode ser influenciada pela localização do tumor, extensão da invasão a ligação com estruturas intracranianas vitais etc. Outros fatores clínicos como a idade ou sexo do paciente são fatores preditivos menos importantes nas recidivas.
FONTE: LOUIS, D. et al. WHO Classification of Tumours of the central Nervous System. 4th Ed. IARC: Lyon, 2016.

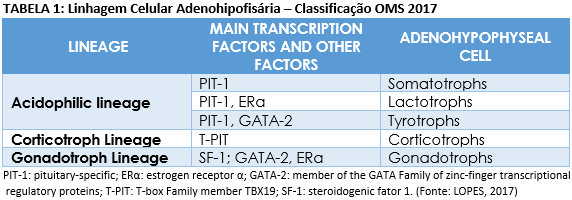
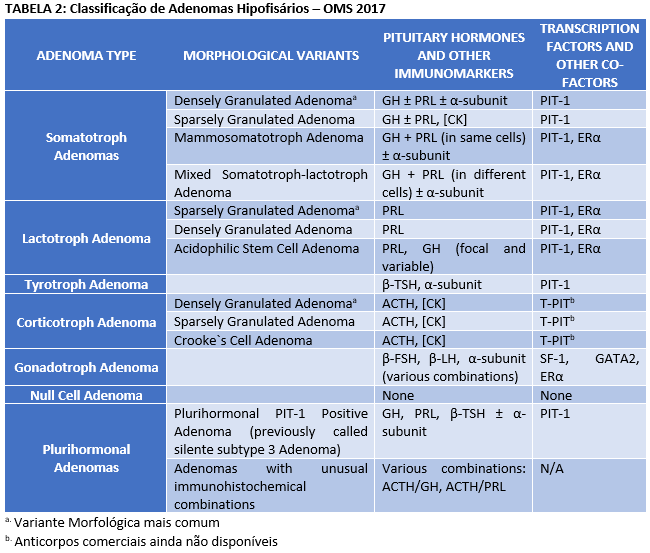
A 4ª edição da classificação de tumores da hipófise da Organização Mundial da Saúde – OMS, publicada em 2017, recomenda diversas alterações na classificação de tumores da hipófise, descreve novas entidades e redefine algumas antigas.
As principais mudanças da nova edição concentram-se na classificação dos tumores da hipófise anterior (adenohipófise). Estas alterações incluem (1) uma nova abordagem para a classificação de tumores neuroendócrinos de acordo com a linhagem das células adenohipofisárias; (2) alteração na graduação dos tumores neuroendócrinos hipofisários com eliminação da nomenclatura “adenoma atípico”; (3) introdução de novas entidades como Blastoma Hipofisário e redefinição de antigas entidades como o adenoma de células nulas.
Nas últimas décadas, diversos fatores de transcrição e outros fatores de diferenciação hipofisários foram descobertos. Esta nova classificação traz informações de grande relevância terapêutica e prognóstica. A nova classificação utiliza a linhagem celular como forma de categorização. Esta nova classificação é baseada em estudos imunohistoquímicos e outras colorações especiais destinados aos hormônios hipofisários, sendo esta a principal ferramenta diagnóstica para este tipo de tumor no momento.
FONTE: LOPES, M. Beatriz S. The 2017 World Health Organization classifiction os tumors of the pituitary gland: a summary. Acta Neuropathol., n. 134, p. 521-535. Springer-Verlag GmbH Germany 2017.

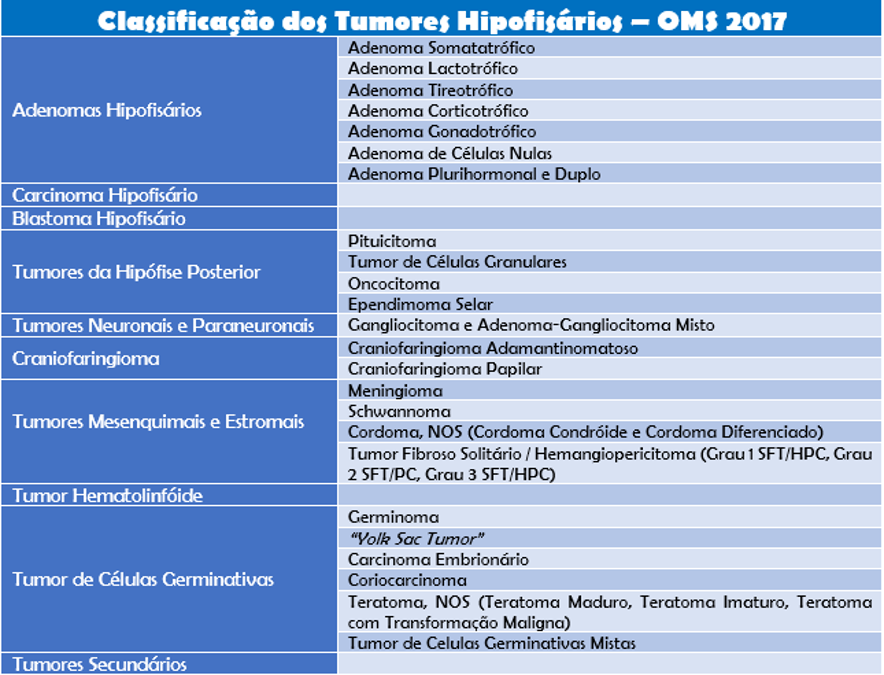
A maioria dos tumores hipofisários são pouco agressivos, mas podem causar diversos transtornos ao alterar a produção de hormônio de inúmeras glândulas em nosso corpo ou ainda alguns sintomas neurológicos como: visão dupla e perda da acuidade, perda de visão periférica, cegueira repentina, dor de cabeça, dor ou dormência no rosto, tontura, desmaios, etc.
A Organização Mundial da Saúde (OMS) liberou em 2017 uma nova classificação de tumores hipofisários. Esta nova classificação oferece informações de grande relevância ao tratamento e ao prognóstico do paciente.
A nova classificação é feita preferencialmente de acordo com a linhagem celular ao invés da produção hormonal realizada pela hipófise. Outro ponto importante enfatizado pela nova classificação é a definição da imunohistoquímica em combinação com outras colorações especiais como as principais técnicas necessárias à sua classificação.
Esta nova classificação ficou mais prática, fornecendo informações definitivas ao diagnóstico e valiosos dados prognósticos que auxiliam muito na orientação do tratamento a ser definido pela equipe médica. Lesões mais agressivas devem ser identificadas com base na histopatologia, índice mitótico, índice de marcação do anticorpo Ki-67, bem como a infiltração do tumor nas demais áreas cerebrais.
FONTE: LOPES, M. Beatriz S. The 2017 World Health Organization classifiction os tumors of the pituitary gland: a summary. Acta Neuropathol., n. 134, p. 521-535. Springer-Verlag GmbH Germany 2017.
Os Ependimomas são tumores intracranianos e medulares que ocorrem tanto em adultos quanto em crianças. Nos EUA, cerca de 30% de todos os tumores do Sistema Nervoso Central (SNC) encontrados em crianças menores de 03 anos são ependimomas. A incidência diminui com o aumento da idade do paciente. Quando localizados na Medula Espinhal, os ependimomas são a neoplasia neuroepitelial mais comum, representam cerca de 50-60% de todos os gliomas da medula espinhal dos adultos, sendo mais raros em crianças.
As manifestações clínicas dependem da localização do tumor. Ependimomas da fossa posterior podem apresentar sintomas de hidrocefalia e aumento da pressão intracraniana, causando dores de cabeça, náuseas, vômitos e tontura. Quando envolve estruturas cerebelares e o tronco cerebral pode causar ataxia, distúrbios visuais, paresia, ou déficits de nervos cranianos.
Pacientes com ependimomas supratentoriais podem demonstrar déficits neurológicos focais ou epilepsia, bem como aumento da pressão intracraniana. O aumento da cabeça ou separação das suturas cranianas podem ficar evidentes quando encontrados em bebês. Ependimomas localizados na medula espinhal podem apresentar dores nas costas, déficits sensoriais e motores ou paraparesia.
Ependimoma é um glioma bem delimitado, composto de pequenas células com núcleos redondos dispostos em uma matriz fibrilar. É caracterizado por zonas perivasculares anucleadas (pseudo-rosetas) com rosetas ependimais também encontradas em aproximadamente um quarto dos casos. O ependimoma clássico geralmente possui baixa densidade celular e baixa proliferação. Raramente invade áreas adjacentes ao SNC.
A definição precisa de anaplasia em um ependimoma é essencial ao prognóstico. Recentemente foram identificados nove grupos moleculares para os ependimomas, auxiliando na triagem de terapias adjuvantes e na identificação do prognóstico. Por isso, um diagnóstico preciso é determinante para o sucesso do tratamento. O diagnóstico confiável pode determinar se a remoção cirúrgica foi suficiente ou se há necessidade de terapias adjuvantes à cirurgia.
FONTE: LOUIS, D. et al. WHO Classification of Tumours of the central Nervous System. 4th Ed. IARC: Lyon, 2016.
O grupo de doenças neuromusculares engloba doenças que acometem os músculos, a placa motora e os nervos periféricos. Estas doenças podem ter causas adquiridas ou genéticas, e esta elucidação é essencial para seguimento do tratamento. O diagnóstico de doenças neuromusculares é considerado difícil, mas na maioria dos casos um exame clínico cuidadoso e algumas rotinas laboratoriais mais específicas podem auxiliar esta tarefa.
A Biopsia Muscular possui um papel muito importante como parte do processo diagnóstico de um paciente com algum tipo de doença neuromuscular. Um diagnóstico preciso e a identificação de uma característica estrutural patogênica leva a uma melhor conduta médica, trazendo uma resposta mais decisiva ao paciente e contribuindo com informações prognósticas importantes.
Em geral, a principal indicação para a biopsia muscular é alguma evidência de doença muscular como fraqueza muscular, cãibras ou desconforto e fadiga muscular por algum tipo de atividade. A seleção do músculo a ser biopsiado é baseada de acordo com a distribuição da fraqueza muscular, possibilitando visualizar possíveis alterações nos músculos avaliados. O procedimento é realizado sob anestesia local, retirando um pequeno fragmento de músculo afetado. O paciente é liberado logo após o procedimento e pode retomar sua rotina em seguida.
A Biopsia Muscular é um procedimento que exige um processamento específico do material coletado. A amostra deve ser processada em até 2h após sua coleta a fim de minimizar possíveis artefatos ou a degradação de proteínas e enzimas que possam explicar o quadro investigado. Toda a investigação deve ser realizada em material adequadamente congelado. Fixadores e parafina distorcem a arquitetura da fibra muscular e impossibilitam estudos enzimáticos e metabólicos.
Através do processamento adequado é possível visualizar fibras musculares degenaradas, depósitos de lipídios e proteínas, amiloide, células inflamatórias, deficiência de proteínas importantes para as funções do tecido muscular e outras características que podem interferir no bom funcionamento dessas estruturas.
O resultado obtido é totalmente dependente do processamento realizado no laboratório e da análise e interpretação do neuropatologista, portanto, é essencial procurar por bons profissionais que sejam especialistas neste tipo de análise, garantindo um resultado preciso e uma orientação adequada ao diagnóstico obtido.
Fonte:
DUBOWITZ, V. A SEWRY, C. OLDFORS, A. Muscle Biopsy: A Practical Approach. 4.ed. Elsevier: London, 2013.
GOEBEL, H. A. SEWRY, C. O. WELLER, R. Muscle Disease: Pathology and Genetics. 2. Ed. Neuropath Press: Basel, 2002.
Em muitos tumores do Sistema Nervoso Central, a localização anatômica, os detalhes microscópicos e outros aspectos de sua apresentação clínica possuem forte influência sobre a probabilidade relativa de seus respectivos diagnósticos. Mesmo com tais considerações, os patologistas frequentemente são confrontados com neoplasias que apresentam caracteres morfológicos que restringem o diagnóstico definitivo.
O estudo imunohistoquímico é uma ferramenta complementar que fornece subsídios muito significativos na caracterização de entidades e/ou doenças distintas. As informações adquiridas neste tipo de estudo permitem complementar o que as variáveis morfológicas não permitiram definir com clareza. Assim é possível reconhecer antígenos de superfície, intracitoplasmáticos ou nucleares que são peculiares para cada uma das entidades e alcançar uma conclusão definitiva sobre o diagnóstico.
Este é um método avançado baseado em uma reação antígeno-anticorpo, que produz uma coloração específica quando o anticorpo realiza ligação com o antígeno pesquisado. Pode ser efetuado com material fixado em formol e emblocado em parafina, fornecendo uma grande vantagem quando comparado a outros métodos.
Uma abordagem integrada de estudos imunohistoquímicos e colorações especiais em tumores pouco diferenciados e morfologicamente ambíguos é extremamente relevante para a definição diagnóstica do tumor. Além da caracterização de tumores pouco diferenciados, os estudos imunohistoquímicos também permitem classificar com clareza o grau de agressividade e velocidade de crescimento do tumor em questão, bem como detectar com alto grau de precisão o produto de mutações genéticas importantes para orientação terapêutica, como a mutação TP53 e o IDH, de grande relevância no estudo de gliomas e também eventuais sítios primários em caso de tumores metastáticos.
As análises imunohistoquímicas devem ser adaptadas de acordo com informações como a localização anatômica, características morfológicas e outros aspectos clínicos observados previamente. A correlação com o quadro clínico do paciente pode trazer informações de grande relevância ao diagnóstico e aumentar as chances de sucesso dos tratamentos indicados. Ainda assim, estes estudos são totalmente dependentes da interpretação do patologista, exigindo uma grande base de conhecimento de análise histopatológica.
Portanto, a fim de garantir a definição diagnóstica e aumentar a chance de sucesso dos tratamentos indicados a cada paciente, a Organização Mundial da Saúde (OMS) orienta a realização destes estudos para as análises anatomopatológicas. Mesmo com o avanço das técnicas dos estudos moleculares, estes não substituem as análises imunohistoquímicas. Os diferentes métodos diagnósticos devem ser usados seletivamente, a critério do patologista, para fornecer soluções efetivas e abrangentes à casos específicos.
FONTE: WICK, MR. Immunohistochemical approaches to the diagnosis of undifferentiated malignnt tumors. Annals of Diagnostic Pathology, n. 12, p 72-84, 2008.